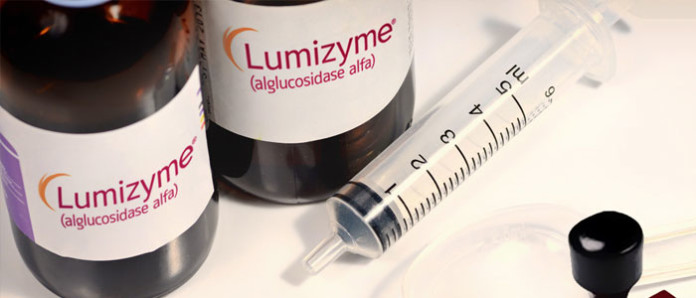

La FDA de EE.UU. ha anunciado la aprobación de Lumizyme (alglucosidasa alfa) para el tratamiento de pacientes con enfermedad de Pompe infantil, incluidos los pacientes que tienen menos de 8 años de edad. Además, la Estrategia de Evaluación de Riesgos y Mitigación (REMS), conocido como el Programa de Lumizyme ACE (Alglucosidasa Alfa Control y la Educación) está siendo eliminado.
La enfermedad de Pompe es una enfermedad genética rara y ocurre en un estimado de 1 de cada 40.000 a 300.000 nacimientos. Su síntoma principal es el corazón y debilidad del músculo esquelético, de progresar a debilidad respiratoria y la muerte por insuficiencia respiratoria.
La enfermedad causa mutaciones genéticas para impedir que el cuerpo produzca suficiente de la forma funcional de una enzima llamada alfa-glucosidasa ácida (GAA). Esta enzima es necesaria para el adecuado funcionamiento muscular. GAA es utilizada por las células del corazón y de los músculos para convertir una forma de azúcar llamada glucógeno en energía. Sin la acción de la enzima, el glucógeno se acumula en las células y, en última instancia, debilita el corazón y los músculos. Se cree Lumizyme a trabajar mediante la sustitución de la GAA deficiente, reduciendo de ese modo la glucógeno acumulado en el corazón y células del músculo esquelético.
Lumizyme, un glucógeno específica enzima lisosomal, fue aprobado por la FDA en el año 2010 con un REMS para restringir su uso para el tratamiento de pacientes con enfermedad de Pompe tarde (no infantil) inicio que son 8 años de edad y mayores. El REMS fue necesaria para reducir el riesgo potencial de progresión rápida de la enfermedad en el inicio en la infancia los pacientes con enfermedad de Pompe y los pacientes con enfermedad de inicio tardío de menos de 8 años de edad, y para comunicar los riesgos de anafilaxia, reacciones alérgicas severas y graves de la piel y sistémica inmune mediada reacciones a los prescriptores y los pacientes.
En el momento de la aprobación de Lumizyme, no hubo datos suficientes para apoyar la seguridad y eficacia de Lumizyme en la población de Pompe inicio infantil, por lo Lumizyme fue aprobado para su uso sólo en los pacientes con enfermedad de inicio tardío de Pompe que tengan al menos 8 años de edad. Pacientes con enfermedad de Pompe de inicio infantil y pacientes menores de 8 años de edad continuaron el tratamiento con Myozyme, que ya fue aprobado. Myozyme y Lumizyme, ambos fabricados por Genzyme Corporation, se producen a partir de la misma línea celular a diferentes escalas de producción.
Esta aprobación permite el acceso a Lumizyme para todos los pacientes de la enfermedad de Pompe, independientemente de su edad.
La FDA revisó la nueva información disponible y determinó que Lumizyme y Myozyme son química y bioquímicamente comparable. En consecuencia, se espera que la seguridad y la eficacia de Myozyme Lumizyme y ser comparables. Además, un estudio clínico de un solo centro de 18 inicio en la infancia los pacientes con enfermedad de Pompe, de entre 0,2 a 5,8 meses en el momento de la primera infusión, proporciona más apoyo que los pacientes inicio en la infancia tratados con Lumizyme tendrán una mejora similar en sin ventilación supervivencia como aquellos tratados con Myozyme.
Dado que los datos se presentaron apoyar la aprobación de Lumizyme para todos los pacientes de Pompe, una REMS restringir su uso a un determinado grupo de edad ya no es necesario. Aunque el riesgo de anafilaxis, reacciones alérgicas graves, y cutáneas severas y reacciones mediadas inmunes para Lumizyme todavía existen, estos riesgos son comparables a Myozyme y se comunican en el etiquetado a través de las advertencias y precauciones, y un recuadro de advertencia.
«REMS siguen siendo instrumentos esenciales para el organismo que emplea a medida que trabajamos con las empresas para hacer frente a los graves riesgos asociados con las drogas y controlar su uso apropiado y seguro en diversos centros de atención de salud», dijo Janet Woodcock, directora del Centro de la FDA para la Evaluación e Investigación de Drogas. «La agencia mantiene su compromiso con el ejercicio de un enfoque reglamentario flexible y responsable que asegure que los programas REMS están siendo eficaz y eficientemente utilizados y que no resulte en una carga innecesaria a los profesionales sanitarios y los pacientes.»
Los profesionales sanitarios y los pacientes deben ser conscientes también:
La sección Advertencias y precauciones de la etiqueta del producto Lumizyme y la sección de Estudios Clínicos de la etiqueta Lumizyme se han actualizado para incluir la información de seguridad del medicamento en inicio en la infancia los pacientes con enfermedad de Pompe. Esto incluye la información de la etiqueta Myozyme actualmente aprobada y la información de un nuevo estudio, no controlado en el que los pacientes con enfermedad de aparición infantil fueron tratados con Lumizyme.
Lumizyme se aprueba con un recuadro de advertencia por el riesgo de anafilaxis, reacciones alérgicas graves, reacciones autoinmunes e insuficiencia cardiorrespiratoria.
Los profesionales sanitarios deberán continuar haciendo referencia a la información sobre medicamentos de prescripción para las últimas recomendaciones sobre la prescripción Lumizyme y reportar eventos adversos con el programa MedWatch de la FDA (http://www.fda.gov/Safety/MedWatch/default.htm).
Distribución de Lumizyme ya no estará restringida. Profesionales de la salud, centros de salud y los pacientes ya no serán obligados a inscribirse en el programa Lumizyme REMS (Programa ACE Lumizyme) para poder prescribir, dispensar o recibir Lumizyme.
Los efectos secundarios más comunes de Lumizyme fueron las reacciones relacionadas con la infusión y se incluyen reacciones alérgicas severas, urticaria, diarrea, vómitos, dificultad para respirar, picazón en la piel, erupción cutánea, dolor de cuello, pérdida parcial de la audición, sofocos, dolor en las extremidades, y el pecho malestar.
Myozyme y Lumizyme son comercializados por Genzyme con sede en Cambridge, Massachusetts,.
farmacos para curar la enfermedad de pompe, medicamentos para prevenir el pompe, nombre medicamento Genzyme para tratar Pompe