
Los científicos de The Scripps Research Institute han descubierto un método sorprendentemente simple y seguro para interrumpir genes específicos dentro de las células. Los científicos destacaron el potencial médico de la nueva técnica mediante la demostración de su uso como una alternativa más segura a una terapia genética experimental contra el VIH.

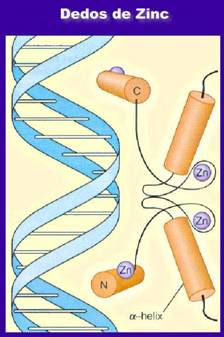
La nueva técnica, publicada en Nature Methods el 1 de julio de 2012, cuenta con nucleasa dedo de zinc (ZFN) las proteínas, que puede atar y cortar el ADN en lugares definidos con precisión en el genoma. ZFNs están llegando a un amplio uso en experimentos científicos y tratamientos potenciales de enfermedades, pero por lo general se entregan en las células usando métodos de genes potencialmente peligrosos terapia.
Los científicos del Instituto Scripps de Investigación simplemente se añaden proteínas ZFN directamente a las células en un plato de laboratorio y encontraron que las proteínas cruzaron en las células y realiza sus funciones de corte de genes con alta eficiencia y mínimo daño colateral.
«Este trabajo elimina un cuello de botella importante en el uso eficaz de las proteínas ZFN como una herramienta de terapia génica en humanos», dijo Michael K. Reddy, quien supervisa las subvenciones de la transcripción del mecanismo de los Institutos Nacionales de Salud (NIH), Instituto Nacional de Ciencias Médicas Generales, que ayudó a financiar la obra, junto con el Premio Pionero de un director de los NIH. «La inmediatez del enfoque del Dr. Barbas de» simplemente «probar la idea de que ZFNs podría poseer una intrínseca penetrante en las células la capacidad es un testamento a su naturaleza altamente creativa y valida aún más su selección como un recipiente 2010 del Premio Pionero de un director de los NIH.»
Cuestionar los supuestos
ZFNs, inventado en la década de 1990, son construcciones artificiales hechas de dos tipos de proteínas: un «dedo de zinc», la estructura que puede ser diseñado para unirse a una secuencia corta de ADN específico, y una enzima nucleasa que cortar el ADN en el que la unión sitio de manera que las células no se puede reparar con facilidad. La tecnología de diseño original para hacer las proteínas dedo de zinc que se utilizan para dirigir las nucleasas de sus genes diana fue inventado por Barbas en la década de 1990.
Los científicos habían asumido que las proteínas ZFN no puede atravesar las membranas celulares, por lo que el método ZFN entrega estándar ha sido una técnica de terapia génica empleando un virus relativamente inofensivo para transportar un gen ZFN diseñador en las células. Una vez dentro, el gen comienza a producir proteínas ZFN ZFN, que buscan y destruyen su objetivo de genes en el ADN celular.
Uno de los riesgos de la aproximación de terapia génica es que el ADN viral, incluso si el virus no es un retrovirus, puede terminar siendo incorporados al azar en el ADN celular, alterando un gen tan valioso como un gen supresor de tumores. Otro riesgo con este método de entrega es que los genes ZFN terminará la producción de proteínas ZFN demasiados, lo que resulta en un elevado número de «fuera de objetivo» cortes de ADN. «El enfoque de la entrega viral implica una gran cantidad de daños fuera del objetivo», dijo Barbas.
En el nuevo estudio, Barbas y sus colegas se puso a buscar un lugar más seguro método de ZFN entrega que no implican la introducción de virus u otro material genético en las células. Ellos experimentaron inicialmente con las proteínas que transportan ZFN segmentos extra de proteínas para ayudarles a penetrar en las membranas celulares, pero no encontró estos ZFNs modificados difíciles de producir en cantidades útiles. Eventualmente, los científicos reconocen que los segmentos de zinc-finger de ZFNs ordinarias tienen propiedades que podrían permitir que las proteínas para obtener a través de las membranas celulares por su cuenta.
«Tratamos de trabajar con ZFNs sin modificar, y he aquí, que eran fáciles de producir y entrado en las células de forma eficiente», dijo Barbas.
Nueva estrategia contra el VIH
A continuación, el equipo mostró cómo la nueva técnica podría ser utilizada en una estrategia ZFN basada contra la infección por VIH.
El retrovirus causante del SIDA normalmente infecta las células T a través de un receptor de superficie celular T llamada CCR5, y la eliminación de este receptor hace que las células T altamente resistentes a la infección por VIH. En 2006, un paciente con VIH en Berlín, perdieron todas las señales de la infección poco después de recibir un trasplante de médula ósea para tratar su leucemia de un donante con una variante del gen CCR5 que se traduce en una baja expresión del receptor. La interrupción del gen CCR5 en las células T con una terapia basada en ZFN podría ser capaz de reproducir este efecto dramático.
«La idea es proteger a algunas de las células T del paciente de VIH, por lo que el sistema inmune sigue siendo lo suficientemente fuerte como última instancia para acabar con la infección», dijo Barbas.
Una terapia génica que utiliza ZFNs para interrumpir los genes CCR5 en las células T y las células modificadas reinfuses T en los pacientes se encuentra actualmente en ensayos clínicos. Barbas y su equipo demostraron que podían lograr el mismo efecto con su simple entrega ZFN método. Añadieron proteínas ZFN directamente a las células T humanas en una placa de cultivo y se encontró que en cuestión de horas, una fracción significativa de las células ZFN tratados mostraron una fuerte reducción en la actividad del gen CCR5.
Después de varias aplicaciones de ZFNs, ayudados por un método de enfriamiento especial que mejora la capacidad de las proteínas para conseguir a través de las membranas celulares, los científicos fueron capaces de inactivar los genes CCR5, con una eficiencia que se aproxima al de la terapia génica basada en enfoque, dijo Barbas.
El nuevo enfoque también parece ser más seguro. Un método basado en el ADN del equipo utilizado para la comparación o los métodos basados en virus reportados en la literatura por otros terminó produciendo ZFNs de hasta varios días, causando una cantidad significativa de daño en el DNA desviado. Sin embargo, las proteínas ZFN entregan directamente se mantuvo intacto dentro de las células de sólo unas pocas horas, causando un mínimo de daños fuera del objetivo.
«En algunos lugares fuera de objetivo en el enfoque de la terapia génica con frecuencia causa daño, no vimos ningún daño en absoluto de esta nueva técnica», dijo Barbas.
El equipo probó su directa técnica de entrega ZFN con una variedad de otros tipos de células y hallaron que funciona con una eficiencia particularmente elevada en los fibroblastos de piel humana «,» las células. Los investigadores ahora están trabajando en terapias avanzadas en las que se cosechan los fibroblastos de pacientes con este tipo y reprogramar las células de los patrones de expresión genética para que éstos se conviertan en células madre. Estas células madre inducidas se pueden modificar mediante ZFNs y otras técnicas de edición del genoma. Cuando se vuelven a infundir en un paciente, que puede producir millones de células de la progenie terapéuticas durante largos períodos.
Estas técnicas pueden usarse algún día para tratar una amplia gama de enfermedades. Barbas, quien ha sido el desarrollo de las estrategias anti-CCR5 durante más de una década, quiere comenzar con una terapia basada en ZFN que interrumpe el gen CCR5 en las células madre hematopoyéticas. Estas células sanguíneas de toma de células madre, a infundir en un paciente con VIH, se convertiría en pequeñas fábricas para la producción de VIH resistentes a las células T.
«Incluso un pequeño número de células madre que llevan a esta característica de resistencia del VIH podría llegar a sustituir completamente a un paciente de la población de células T original y vulnerables», dijo.
alternativas a la terapia genica, articulo cientifico sobre el virus del vih como herramienta de terapia genica, carlos barbas biólogo molecular, cientificos y terapiagenica